https://youtu.be/1W-_WT7k-IA
フッ素を使わない理由とは?
従来言われているフッ素の効果とは?
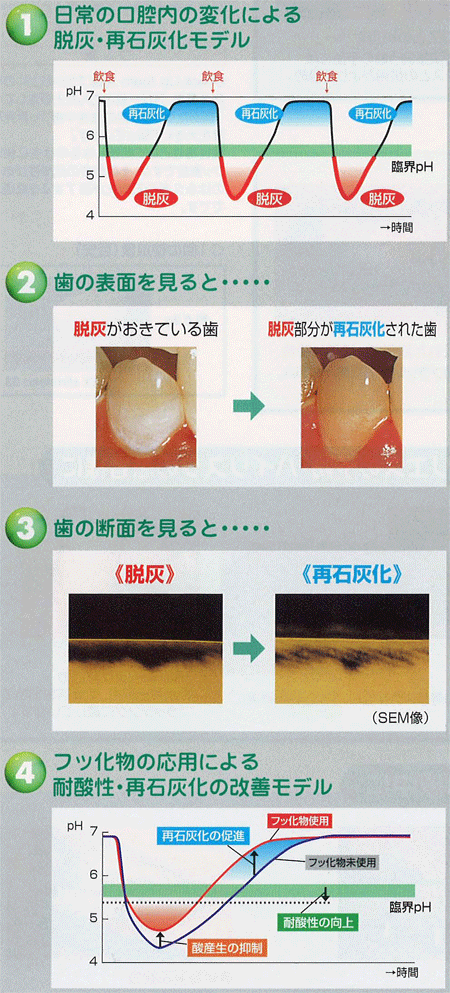
さてフッ素と聞くとどんなイメージをお持ちになりますか? フッ素は現在虫歯予防に良いという観点から、歯磨き粉に添加されたり、歯科院で塗布したりして、広く使われています。
つまりフッ素が歯に作用すると溶け出したミネラルの歯の修復をしたり、歯の結晶構造に取り込まれ、フロールアパタイトという固い歯質になり虫歯を予防するというのが、定説になっています。
フッ素の虫歯予防の効果を覆す報告
しかしながら、その定説を覆す研究が有りました。その研究では、フッ素推進派の方々が、進める理由として挙げている効果である歯質強化はありえない!
↓
生体アパタイト結晶形成構造とフッ素イオンの影響
http://www.ctb.ne.jp/~kazuno/Kakei.pdf
(以下はその本文より抜粋しています)
「はじめに、顕微ラマン装置を用いてフッ素処理した歯と合成アパタイト結晶にフロール化が本当に生じているか否かについて分析結果を報告する。
結果は処理時間にかかわらずメディアを通じて宣伝されているような結晶構造中におけるフッ素イオンの置換は認められずフロール化は起こっていない。 当時は、結晶構造の変化を直接分析できる高性能な装置は無く 、試料中におけるフッ素量増加の 分析結果を基に推測 したにすぎなかったが、フッ素処理することでより難溶性のフロールアパタイトが形成されるとして多くの研究者に受け入れられて、今日に至っている。
さらに、顕微ラマン分析装置の出現にもかかわらず 、現在予防歯科で行われている処理方法で作成した試料のラマンデータの分析報告が見当たらない。 むしろ、論文に記載されている試料の処理過程は、 歯科で行われている虫歯予防処理とはるかにかけ離れ、非現実的である。 ・・・」
「1.J.F. Volker, Proc. Soc. Exp. Biol. Med. 1939(42) 725-727
残念ながら、筧先生も指摘していらっしゃるように電子機器が発達した現在でも、ラマン顕微のデータの分析報告はなされていない様子です。それはなぜなんでしょうか?
フッ素神話の歴史
さて、フッ素が医療従事者や市民にとって安全だと信じ込ませる事でどんな利権が絡んでいたのか、その歴史を振り返ってみたいと思います。記事にするにあたり、村上 徹先生のHPやTHINKERさんのHPを参考にさせていただきました。(ありがとうございます)歯磨き粉などに添加されているフッ素は残念ながら毒物です。ではなぜそんな毒物が、虫歯予防に使われるようになったのでしょうか?
なぜ だれが どうして
そもそもフッ素の有効利用の始まりはアメリカにおけるアルミニウム産業でした。産業廃棄物であるフッ素の毒性と処理に手を焼いていたアルコア社の主任研者フランシス・フレイリーは、メロン産業研究所の研究員ジェラルド・コックスにフッ素の歯に与える影響を研究して、その有効利用を提案しました。そして、コックスは1939年に虫歯予防のために、公用の水道水にフッ素を添加することを提唱します。また、このメロン産業研究所は、アルコア社の株主であるアンドリュー・メロンが設立したもので、真の目的は、大企業が起こす大気汚染・土壌汚染などの公害に対して行われる訴訟から産業を守るために有利なデータを作成すること でした。同社はアスベスト産業を守るために「アスベストは安全である」と 長年主張し続けています。その後、欧米において「宣伝広告の父」との異名をもつ、エドワード・バーネイが「虫歯予防にフッ素」というキャッチフレーズで水道水へのフッ化物添加キャンペーンをテレビ・ラジオ・ポスターなどを用いて全米で大々的に展開しました。そして、「フッ素は安全なもの、体に良いもの」というイメージが一般社会に定着したのです。
フッ素の恐ろしい歴史
アメリカでは全人口の70%の公用水道水ですでにフッ素化合物が添加されています。そのため、住民のフッ素に対する関心も高いのです。
1950年代、アメリカで水道水へのフッ素化合物添加の是非を巡る一大論争が科学者の間で起きました。そのとき低濃度(1ppm=100万分の1)のフッ素の安全性を訴えたフッ素支持派の筆頭者はハロルド・ホッジ博士でした。恐ろしいことに、ホッジ博士とは、広島に投下した原子爆弾を開発した「マンハッタン・プロジェクト」の中心人物であり、その他にも数々の非人道的な実験を行っていたことでも有名ですが、詳細は後述します。
史上最大の汚染物質
大気汚染物質として知られる数多くの化学物質の中でも、フッ素は最も危険であることがわかっており、さまざまな機関がフッ素の有害性を訴えています。安全とされる適量のフッ素を投与しただけで神経細胞から、他の神経毒が引き起こすような多動性障害、記憶障害、知能障害の典型的な画像パターンが観測された のです。
YouTubeでフッ素が神経毒という証拠の動画が見られます。
VIDEO
以下本文より一部抜粋
ユニセフ(国連国際緊急児童基金)が、1999年12月に飲料水のフッ素の安全性について、疑念をあらわすレポートを公表した。
このようにフッ素については、実に恐ろしい歴史がありそうです。さらに詳しく調べてみたい方は、村上先生のフッ素毒警告ネットワークでお調べください。http://www.ctb.ne.jp/~kazuno/f-link-murakami.htm
最近のアメリカのフッ素事情
―以下ナチュラルニュース本文の訳―
アメリカでの水道水へのフッ素添加は1945年に始まり現在に至る。
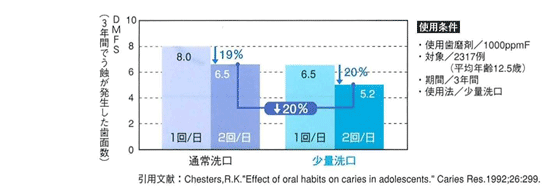
アメリカでのフッ素の水道水への添加が始まる1年前より、歯学の専門家たちはほぼ全員揃って、フッ素が歯の健康にとって有害な事を認識していました。事実1944年のアメリカ歯学協会の雑誌に、1.6~4ppmの濃度のフッ素を水道水に添加する事で、成人の半数が歯牙の補綴が必要になる事を報告していました。その確固たる証拠は、生徒たち40万人を対象にした世界でも最も大規模な調査により、1ppmのフッ素添加の水道水を飲用する事で、25%虫歯が増加する事が明らかにされていることです。
まだ1945年にはフッ素はニューバーグ、ニューヨーク、そしてグランド・ラピッズ、ミシガンなどの自治体で添加されているだけでした。あれから50年今では60%のアメリカ人が1ppmのフッ素を添加された地域に住み、現在75%のアメリカの州でこの致死的な毒が水道水に含まれています。
偽作のうちの1つは「フッ素が歯の結晶構造の構築を助ける」という事です。しかしそれは「アメリカのフッ素キャンペーン」から早々と削除されました。このキャンペーンは全くの嘘であると認識され、暴露されていますが、FDAとCDCは単にこの一文の削除だけをして、いまだに大衆にはフッ素が虫歯予防に良いと信じ込ませようとしています。
いまだにアメリカ人の70%がこの多角的な神話を信じています。
フッ素が他の国でどのように使われているか考えてみましょう?
フッ素はお水を浄化しますか?
フッ素は虫歯を予防して骨を強化するか考えてみよう?
フッ素が水から蒸発するか考えよう?
ADAは歯科の専門家たちを締め付けているので、フッ素の真実について公表する歯科医は皆無です。ADAは歯科医の免許をはく奪する機関である国家歯科医院会に影響力を持っています。それで、あなたは歯科医からフッ素についてのネガティブな情報を得る事が無いのです。
フッ素はFDA(アメリカ食品医薬品局)の認可をまだ取っていない
それではいったいなぜアメリカの規制機関はこの悪夢の永続を許したのでしょうか?
ほうろう、陶器の顔料、殺虫剤フッ素の意外な用途を知っていますか?
さて、フッ素はセラミックの顔料、水道水への添加、ほうろう、核産業、紙産業、農業で使われる殺虫剤など実に様々な用途で使われています。実に恐ろしい話です。
中国のフッ素の供給者を明らかにする証拠(フッ化ナトリウムは殺虫剤、防腐剤として使われる)
フッ素の推進の医者や歯医者はあなたの水道水をフッ素に汚染させる事で、賢い嘘に塗り固められた致死的な目的を果たそうとします。その嘘とは全てのフッ素擁護者の間で従順に繰り返されています。それはこういう事です。
「フッ素は水の中にある自然のミネラルです。我々の市では残念なことにフッ素は充分含まれていなく、低いレベルにあります。それで、我々は公衆の健康増進の目的で、その濃度を至適なレベルにする為にフッ素を水道水に加えるのです。」
嘘は殆ど逐語的に至る市で繰り返されており、殆どの市でその毒性のあるフッ素が求められています。なぜそれは嘘なのでしょうか?ここに声明に埋め込まれた5つの嘘が有ります。
嘘1)水道水に加えられているフッ素は天然のものでは有りません。それは中国の化学工場から良く購入している産業廃棄物です。(下に証拠があります)
嘘2)あなたの歯の健康に良いといういわゆるフッ素神話は嘘の話です。ベストな事は、フッ素を典型的な治療としてあなたの洗口に使ってそれを吐き出す事です。そしてそれは天然のミネラルとしてのフッ素だけがそうした効果をもち、通常フッ素として推進されているフルオロケイ酸のような毒物ではそうした効果は持ちません。
嘘3)通常市がフッ素と呼ぶものは100以上の致死的な化学物質と重金属の毒性のある混合物です。それは通常中国の工場の産業の過程で発生するものでフッ化ナトリウムと言うラベルと貼られて毒性の強い産業廃棄物として持ち出され、購入されます。
嘘4)水道水中のフッ素の濃度が低いとかフッ素の至適濃度などと言う話はどこにも有りません。そもそも純粋な飲料水にはフッ素は含まれていません。
嘘5)フッ素は人間が飲んでも安全だと言いますが、本当でしょうか?それであればなぜフッ化ナトリウムは産業界の製造工場によって、人にとって重大な危害を及ぼすという安全性についての警告のラベルが貼られるのでしょうか?
中国のフッ素の製造者はそれが毒性のある化学物質である事を認めました
いわゆる沢山のフッ素がアメリカ、カナダ、オーストラリアなど他の国々で公衆の水道水に中に捨てられています。そしてそれは実際中国の例えば雲南省のフッ素化学会社等の会社から来ています。
あなたがアリババ.comのページにある化学工場のリストを見るとハッキリするかもしれません。そのユーザーの為の記述によればフッ素化学雲南社は98%のフッ化ナトリウムの製品を提供しています。
それはスチールを発泡(エファバシング?)させるときに使ったり、製錬したり、軽金属を精錬するときに使います。それは飲料水をフッ素化する時にも使いますし、木の防腐剤、防腐剤入りの接着剤。殺虫剤、メタルの保護のためのコーティング剤、スチールや他のメタルの浸漬剤、はんだ付けや溶接のフラックス、フラックスと同じものがセラミックのおしゃぶりや、ガラスや焼き物の表面に使われます。http://www.alibaba.com/product-gs/540825136/98_min_7681_49_4_for.html )
この会社は合成の氷晶石も製造しており、フッ素の殺虫剤が密かにブドウや他の作物にスプレーされています。あなたの食べ物に大量のフッ素が添加されているのです。http://www.naturalnews.com/036753_fluoride_pesticides_gr%E3%81%97apes.html )
これが合成氷晶石の説明です。それは化学産業の供給者からので、それはアメリカの食物の生産者にトン単位で売られます。
用途:それは単に電気分解で塩と融合したアルミニュウムの精錬の中で溶剤として使われ、ほうろうの製造者に乳濁剤として使われます。乳白剤とほうろうとガラスの溶剤の補助として使われます。作物の殺虫剤としても、アルミニウムの合金を鋳造する際の溶剤としても、そして鉄の合金やスティールの発泡(エファバシング)の時にも。また耐磨耗性のある樹脂やタイヤの研磨剤としても同様に使われます。
それは人の皮膚を高度に腐食させます。
もう一つの市政の水道施設のフッ化ナトリウムの供給者は、中国の上海ポリメット・コモディティズ株式会社です。ある程度の量フッ素の化学物質の供給をしています。
フルオロケイ酸・けいフッ化水素
性質・無色、透明、揮発性の液体で著しい臭気を伴う、強酸性で、水溶性で、揮発性、消毒作用が有り、セラミックのガラス、鉛と他の金属を腐食し、人間の皮膚をひどく腐食させ人の呼吸器系に害を及ぼします。プラスチックから出来ている容器にそれを入れておきましょう。http://www.alibaba.com/product-gs/523747967/Fluosilicic_Acid.html )
もう一つの中国のフッ素の供給者はフッ化ナトリウムを農業で使う殺虫剤や殺菌剤として使っている事が示されています。核の産業ではUF2吸着剤として使われています。http://www.alibaba.com/product-gs/421835290/Sodium_Fluoride.html )
他のフッ化ナトリウムの供給者はフッ素の化学物質を無色の結晶もしくは白い粉として使う事が記述されていて、それは毒性を持っていて水に溶解します。http://www.alibaba.com/product-gs/264259230/Sodium_Fluoride_NaF_.html )
この会社はフッ化ナトリウムをこんな風に使っていると記述されています。
木材の耐腐食剤、医療腐食、溶接の溶断、スチールの枠の製造、革産業で隠れた処理としてスキンに使われ、防腐接着剤、光のメタルの溶解の精製、着色のフラックスとして
此処に2枚の写真が有ります。アリババのウェブサイトでとったもので、殺虫剤、核工場の化学物質、そして飲料水の化学物質これらの中全てに使われています。
情報源
フッ素の推進者は火地に毒を強要する犯罪者です。
これだけは覚えておいてください。あなたの市の政治家が水道水のフッ素の濃度を自然に存在するフッ素のレベルに合わせていると言っている事を。彼は貴方に嘘を言っています。その本当の意味は彼は水道水に殺虫剤の化学物質を捨ててあなた方全てに毒を飲ませているのです。
この言葉を拡散しよう:フッ化ナトリウムは毒物です!その一つの理由はそれは殺虫剤として有効に働く事です。官僚たちはそれを市の供給水に捨てています。ポートランドの市長のサム・アダムスの様にhttp://www.naturalnews.com/036965_Portland_water_fluoridation_toxic_chemicals.html )
フッ素は化学兵器です。それを摂取すると現実以上の戦時中のコントロール下での副作用を引き起こすことになります。
フッ素はIQの低下を招くという研究
「はい、フッ素は貴方を馬鹿にします」
次回誰かがあなたにフッ素という化学物質が人の健康に悪いという科学的な証拠が何もないと、説得しようとしたら、単に彼らに国立環境学衛生研究所発刊の環境健康展望誌それは現在25刊目ですが、そこに掲載された最近の新しい研究は、「フッ素は脳の発育に障害を与え、著しく人のIQを低下させる」である事を指摘すると良いでしょう。
ハーバード大学の公衆衛生大学と上海の中国医科大学の研究者たちの共同研究は、27の異なったフッ素の研究の評価による「子供たちに対するフッ素の影響」です。そのレビューには、共同チームはフッ素に被爆する事は特に成長期の子供では適正な認知の発達や脳の形成に非常に問題が起こるという「強い影響」を発見しました。
この図によれば、水道水に人工的にフッ素が添加されている地域の子供達は全体的にIQのレベルがフッ素が添加されていない地域に住む子供たちよりも低い事が分かりました。そして他の外部からの認知の健康や発達に影響するであろう因子を考慮した後に、フッ素の被ばくとIQの他メージの関係は否定できない事を結論付けました。
我々の研究結果は子供の神経の発達にとってフッ素の被爆は不利な影響を与える可能性がある事を支持します。と、ハーバード大学の科学研究者のアンナ・チョイと彼女の同僚はこのレポートの中で書いています。フッ素は胎盤に容易に入り込み。成熟した脳よりもより毒物の影響を受け障害を引き起こす事を疑われている発育中の脳が、フッ素に晒される事で永久的にその特性がダメージを受ける可能性を指摘しました。
2010年の発行された同じ医学誌に認知の発達とフッ素の被ばくとに関係性があるとする同様な研究を発見しました。対象となったのは8歳から13歳の中国の2つの農村の子供たちで、一つは水道水にフッ素添加されていてもう一つはフッ素添加されていませんでした。フッ素添加されていた農村と比較するとされていない農村の子供たちのIQレベルが350%全体的に高かったことが明らかにされていました。http://www.naturalnews.com/030819_fluoride_brain_damage.html )
そしてインドでも再度研究者たちがフッ素の化学物質が子供たちの脳内の血液脳関門を通過する事と神経組織の機能と構造に変化を及ぼすことを観察しました。医学誌の「医療と科学同盟」に掲載された特定の研究は、フッ素の普及はいかに脳を含め身体中にフッ素が時間とともに蓄積されていく事に関係しているかを示しています。http://www.naturalnews.com )
特別な利益を得るグループの政治的な目標を満たす為に子供たちに対するフッ素添加の実験を続ける事は理にかなっていません。と、ニューヨーク州のフッ素反対連合の代表で弁護士のポール・ビーバーは言います。「もしフッ素が虫歯を減らしているとしても、歯の健康と脳の健康とどちらが大切か?という事です。そろそろ政策を脇に追いやって、人工的なフッ素の添加を全ての場所で止める時期でしょう。」
食品中に含まれるフッ素
フッ素化・この巨大なる矛盾 訳・脚注・解説・ 医学博士・歯科医師 村上 徹
(転載開始)http://renrakukai.jugem.jp/?eid=51
飲料水の消費量とフッ素の摂取量
フッ素化〔理論〕の基礎構造の弱点は、その計画の心臓ともいえる部分の動脈が広範囲に動脈硬化を起こすまで、時間とともに拡大する。1939年にコックスが産業廃棄物であるフッ素を、虫歯予防のために水道に添加することを提案した時には、水道技術者らは、水道にこれを添加するなら、少なくとも10倍の安全率が必要であると勧告した。現在、魅力的ではない斑状歯が1ppmのフッ素によって至る所で発生している事を思えば、彼等の勧告は、フッ素の望ましい最大許容量は0.1ppmであり、1.0ppmというのはそれだけで否定するに足る十分な理由となるだろう(5)。
表19-1 フッ素化による1日あたりの平均フッ素摂取量の見積もりa 報告年 食物由来のフッ素 水量 飲料水由来のフッ素b 総摂取量 最初の報告者(文献番号) 1943c 0.03-0.56mg 0.4-1.2l 0.4-1.2mg 0.4-1.7mg マックルーア(9) a b c
その4年後に、彼らはそれを1.5ppmに引上げた(7)。明らかにその根拠となったのは、局の研究者であったマックルーアが、5人の健康な男子について行った次のような研究である。「1.8~1.9ppmのフッ素を含有する飲料水や、3.0~4.0mgの1日あたりのフッ素の平均摂取量を来すような飲料水が、蓄積性のフッ素中毒症の流行をもたらすことはない」(8)。この論文は、同時に次のようにも述べている。4.0~5.0mgのフッ素は「1日あたりの摂取量としては、体内に貯留しても障害を起こさない限界量である。」
飲料水の消費量と、飲料水と食品から摂取する1日あたりの平均フッ素料に関する1940年代のマックルーアの見積もりは、表19-1に示したとおりである。現在、合衆国で1961年に定められたフッ素化の基準である0.7~1.2ppmという濃度は、この数値に気温の効果を加味したものに基づいている。公衆衛生局によれば、この濃度でも2倍の安全性があるという。と言うのも、〔彼らの見解では〕フッ素の最大許容量は1.4~2.4ppmだからである(15)。しかし、この濃度はディーンが夥しい数の歯牙フッ素症に遭遇した濃度だ(16)。さらに追加して言うなら、食物からくるフッ素量を0.5mg/日と低く見積もっても、2.4ppmのフッ素化水を毎日1.5リットル飲むとすれば、その量は3.6mg/日となり(17)、これでは簡単にマックルーアが「体内貯留により障害を起こす」とした1日あたりのフッ素摂取量の下限に達してしまうのだ。
さて、次に治療についてであるが、これは何といっても、水、、食品、ドリンク、薬剤、歯磨剤、空気などから体内に侵入するフッ素を厳密に避けることが第一である。しかし、食品とくに野菜や果物からハロゲンを完全に無くす事は不可能である。これらの食品中のフッ素の量は極めてマチマチで、栽培された場所、調理の仕方、肥料や〔農薬の〕スプレーの程度、汚染された環境からの曝露の程度などによって大きく異なる。さらに茶葉、魚(とくに骨)、鶏肉の皮、チョコレートもフッ素濃度が高いのがふつうである。おそらく、フッ素含有量が最も少ない食品は、ミルク、卵、精肉の赤身(内臓を除く)、保護皮を持っている植物の製品(メロン、レモン、バナナ、ココナッツの類)、それ自身のジュースの中にパックされている果物(パイナップル)、非フッ素化地区の外国や低フッ素化地区で製品化された缶詰などである。一般的に言って、缶詰は色々な原因からフッ素濃度が極端に異なる。フッ素に不耐性な人はよく注意して食品を調べ、もし、それを使った後で症状が出るようならば他のブランドのものに換えなければならない。
日弁連から集団フッ素洗口・塗布の中止を求める意見書が出されています
このサイトから、日本弁護士連合会が出している集団フッ素洗口・塗布の中止を求める意見書がダウンロードできます!http://www.nichibenren.or.jp/library/ja/opinion/report/data/110121.pdf
フッ素についての10の真実
フッ素についての10の真実1.pdf
ダウンロード
VIDEO
フッ化ナトリウム安全データシート(昭和化学)
ダウンロード
 フラッシュパールの特徴
フラッシュパールの特徴

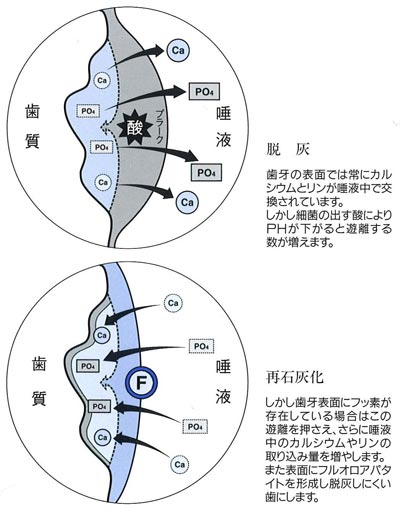












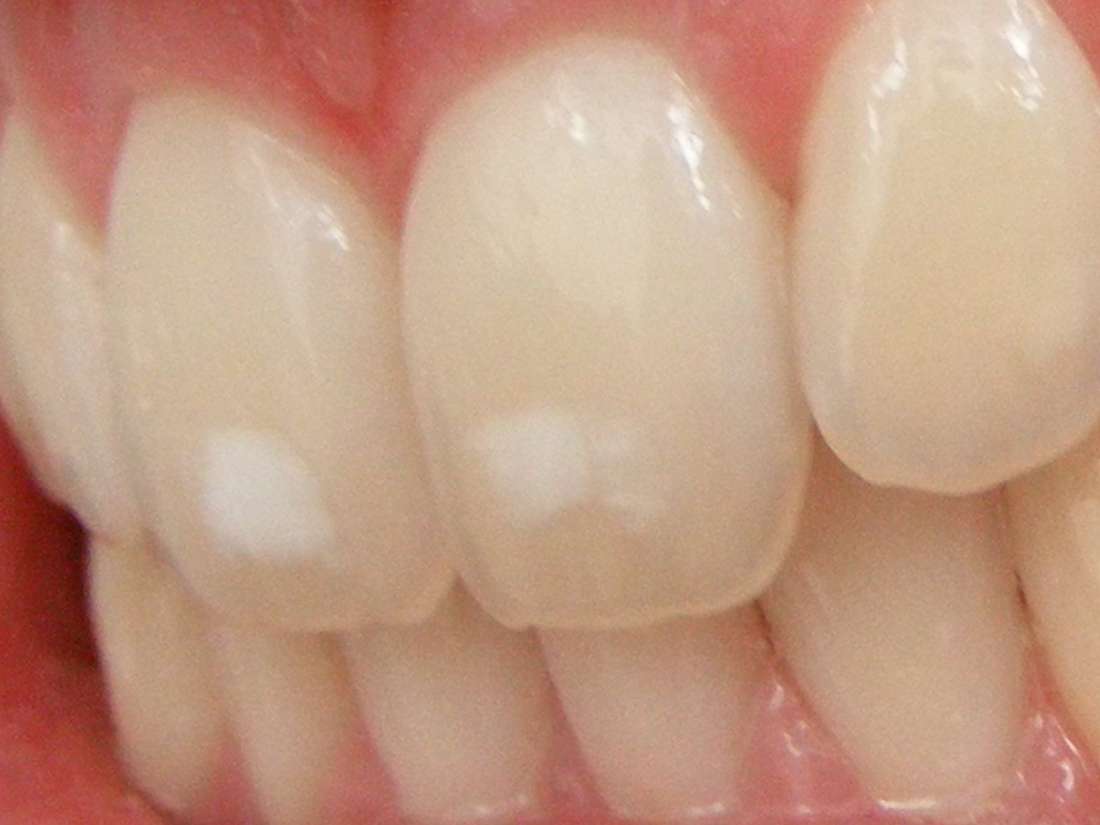



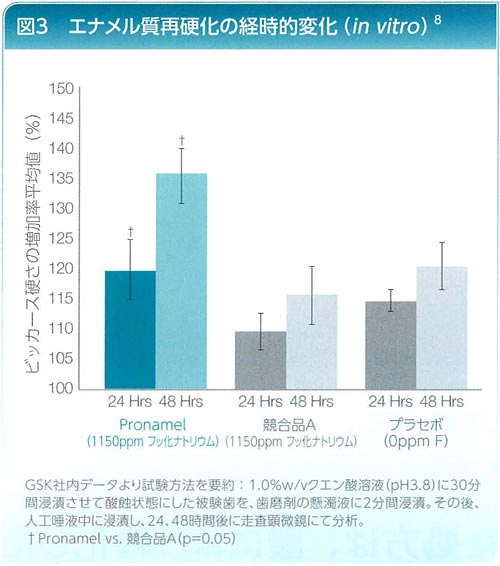
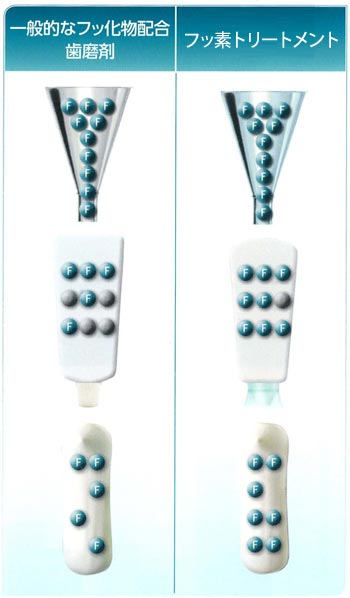

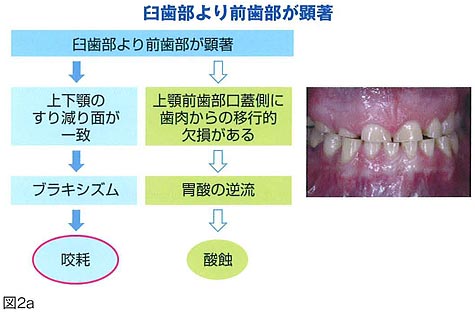
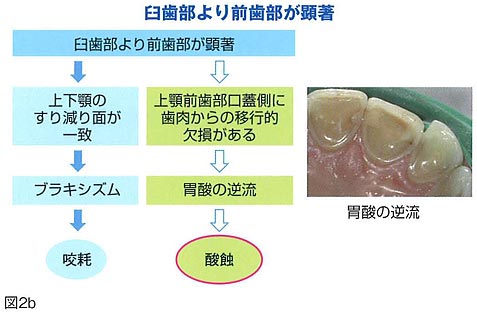










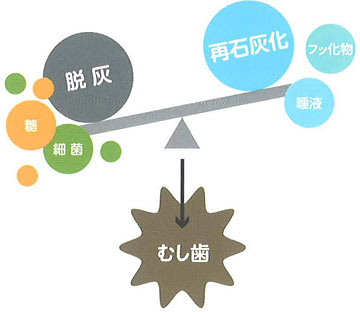
 歯質を強くします
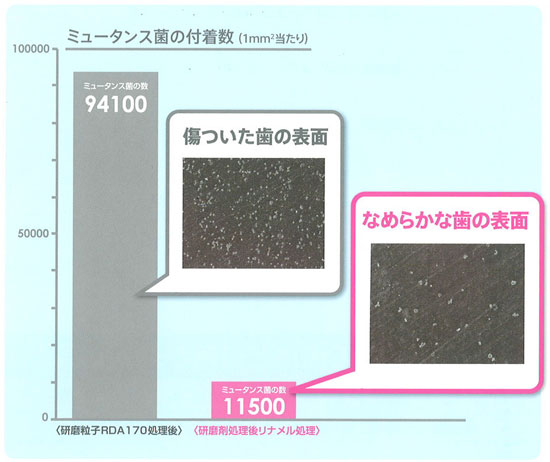
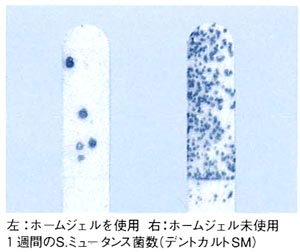
歯質を強くします むし歯菌のはたらきを抑えます
むし歯菌のはたらきを抑えます